Le plateau technologique de purification de protéines, installé par l’IGMM au premier étage (pièce 103) a pour finalité d’aider les équipes du site à produire et purifier les protéines nécessaires à leurs travaux de recherche.

Responsable scientifique : Olivier Coux (DR2 CNRS)
Comité de pilotage :
IGMM : Olivier Coux, Odil Porrua, Aude Carusi
IRIM : Mickael Blaise, Jérôme Feuillard
CRBM : Dominique Helmlinger, Céline Faux
L’activité du plateau se déclinera selon 3 axes :
- Production, purification et mise à disposition à terme via le magasin de protéines d’intérêt commun, dans une logique de réduction du coût des expériences.
- Soutien technique aux équipes dans leurs projets de purification de protéines spécifiques. Le plateau prendra en charge la purification dans le cas d’un besoin ponctuel, ou formera un(e) membre de l’équipe afin qu’il ou elle puisse s’autonomiser dans l’utilisation du matériel dans le cas d’un projet « au long cours ».
- Maintien d’une banque de souches d’ coli.
EQUIPEMENT :
Le plateau dispose pour l’instant d’une FPLC et de différentes colonnes de chromatographie (échanges d’ions, gel filtration, interaction hydrophobe) permettant de répondre aux besoins courants de purification de protéines.
CONTACT : pour tout renseignement ou demande spécifique, veuillez-vous adresser directement aux responsables ou contactez-les via l’adresse proteinfacility@igmm.cnrs.fr
Protéines disponibles (*):
| Protéine | Tag | Poids moléculaire | Concentration | Tampon de stockage |
| TEV protease | 6His | 27 kDa | 0,8 mg/mL | 50 mM HEPES pH 7,5 – 1 mM DTT – 45% glycerol |
| Cas9-GFP | – | 191 kDa | 3,7 mg/mL | 20 mM HEPES pH 7,5 – 150 mM KCl – 1 mM DTT – 50% glycerol |
| pAG-Mnase | pAG | 55 kDa | 145 ng/µL | 10 mM Tris pH 7.5 – 150 mM NaCl – 1 mM EDTA – 1 mM DTT – 50% glycerol |
(*): ces protéines seront à terme distribuées via le magasin. Dans l’immédiat, vous pouvez vous les procurer en les demandant directement à Olivier Coux
Procédures et contrôles de qualité :
TEV protease :
La protéase a été exprimée en utilisant le plasmide 6His-pTEV (backbone pET28 – carte disponible sur demande), dans la souche E.coli Rosetta pLysS. Elle a ensuite été purifiée par affinité sur une colonne Ni-NTA, puis par échange d’anions après dessalage. La fraction pure a été centrifugée pour enlever les agrégats et stockée dans 50% glycérol.
Son activité a ensuite été testée en utilisant la Cas9-GFP, qui présente un site TEV entre le tag 6H-MBP et la Cas9-GFP.
L’efficacité de coupure dépend de l’accessibilité du site de fixation de l’enzyme et peut donc varier énormément d’un substrat à l’autre. Nous recommandons d’adapter la quantité de TEV au substrat, en réalisant une gamme en quantité décroissante de TEV à partir de 1 µg de TEV pour 1 µg de substrat.
Analyse de la pureté (Coomassie – 10% acrylamide) :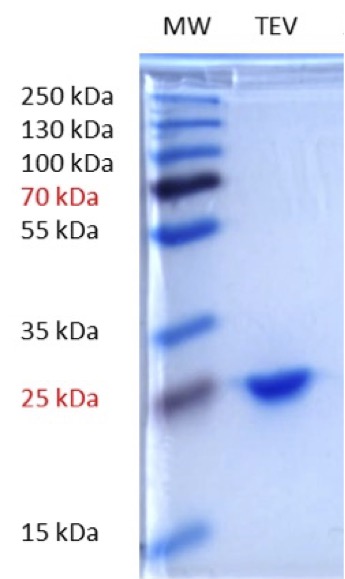
Cas9-GFP
La protéine a été exprimée à partir de la construction 6His-MBP-Cas9-GFP (addgene pMJ922) dans la souche E.coli Rosetta pLysS.
Elle a été purifiée selon les étapes suivantes :
– Affinité sur colonne Ni-NTA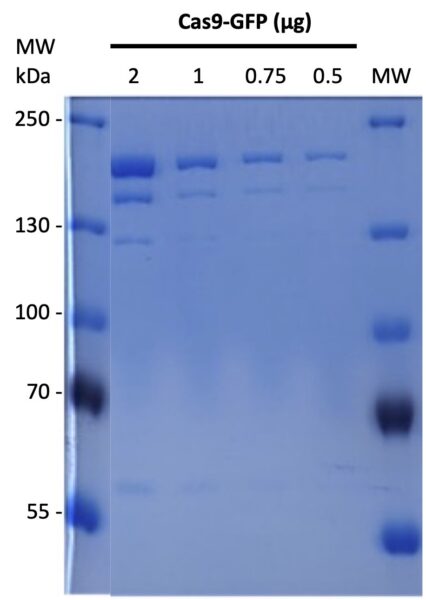
– Elimination de la partie 6His-MBP par clivage avec la protéaseTEV
– Echange de cations sur colonne MonoS
– Gel filtration sur colonne Superdex 200.
Elle a été ensuite concentrée (Vivaspin) à 3,7 mg/mL.
Analyse de la pureté (Coomassie – 8% acrylamide) : ➜
Taille de la protéine : 236K après expression dans E. coli, 191K après élimination des tags
Analyse de l’activité :
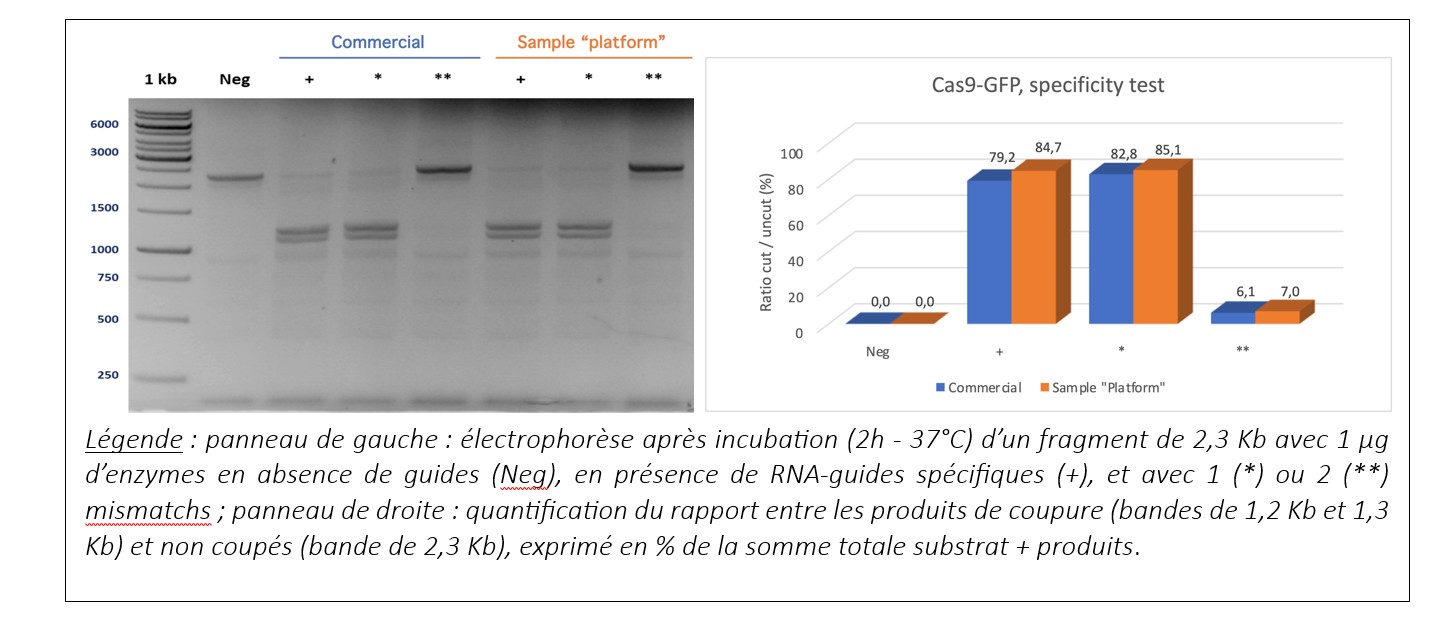
L’activité de la Cas9-GFP a été testée in vitro en la comparant avec une Cas9 commerciale. Deux tests ont été réalisés : un test d’efficacité et un test de spécificité. L’échantillon produit par la plateforme donne des résultats comparables à l’enzyme commerciale.
Efficacité :
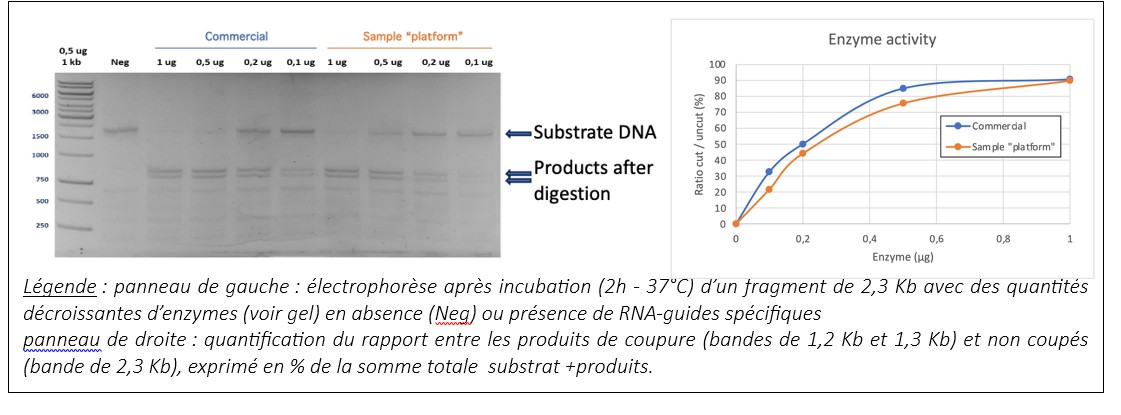
Spécificité :
pAG-Mnase
La protéine a été exprimée à partir de la construction pAG-Mnase (backbone pET28a – carte disponible sur demande) dans la souche E.coli Rosetta II.
Elle a ensuite été purifiée sur colonne IgG, diluée à une concentration de 145 ng/µL, aliquotée et stockée dans 50% de glycerol.
Analyse de la pureté (Coomassie – 15% acrylamide – 2 µg loaded) : ➜
Analyse de l’activité :
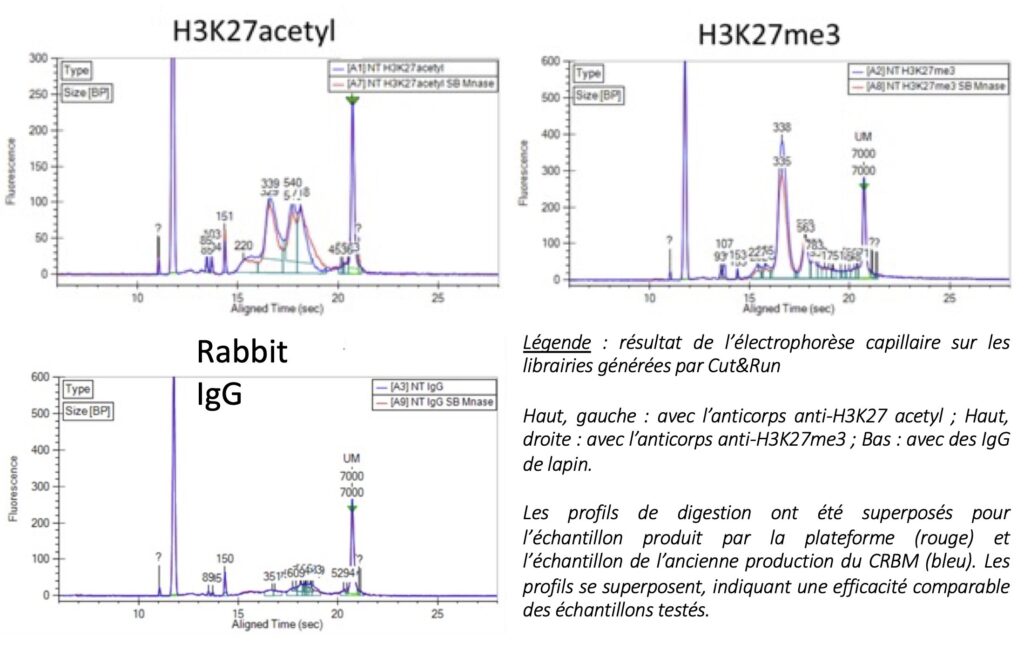
L’activité de la pAG-Mnase a été testée par Cut&Run (Mays Akrouk, équipe GBL – IGMM), en la comparant avec la production actuellement utilisée par différentes équipes (réalisée précédemment au CRBM). Trois anticorps ont été testés, sur des lignées cellulaires leucémiques (AML) : H3K27 acetyl, H3K27me3, et IgG (contrôle négatif). Les librairies Cut&Run générées ont été analysées par électrophorèse capillaire sur la plateforme MGC (CRBM). L’échantillon produit par la plateforme donne des résultats comparables à la production précédente.
Efficacité :
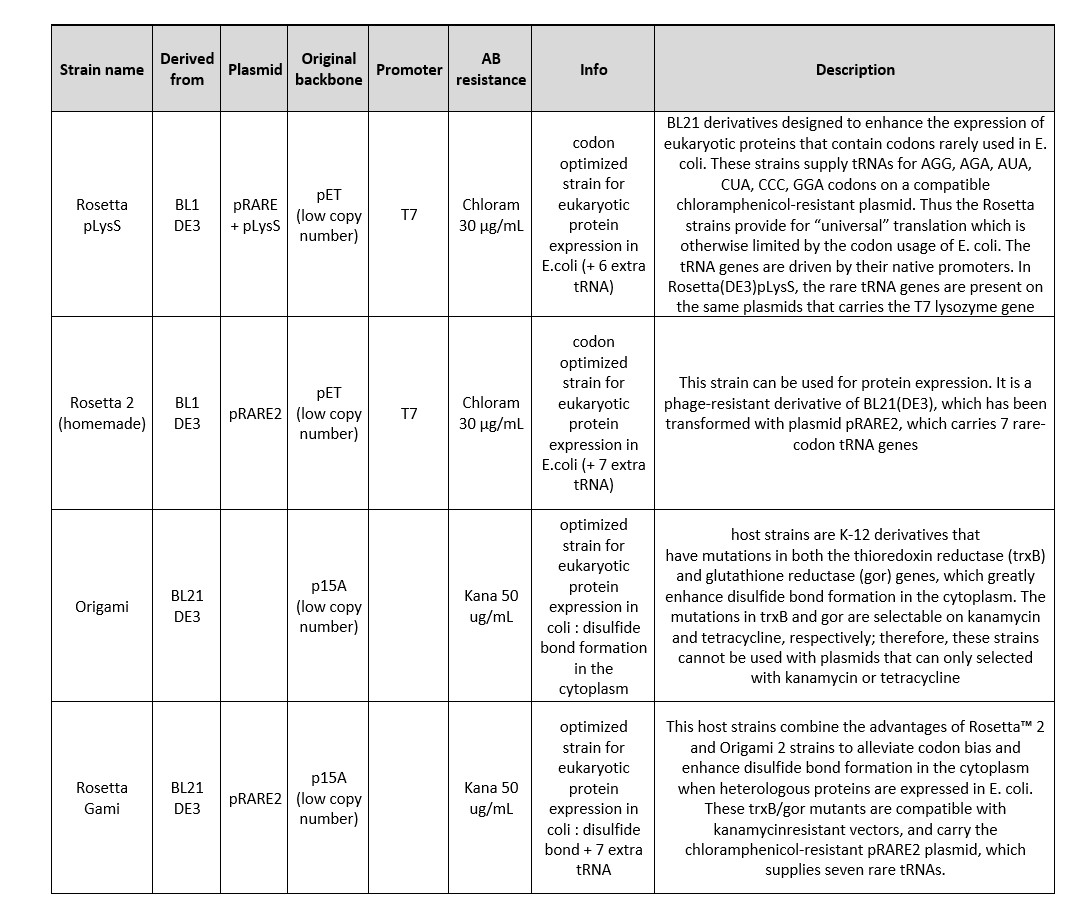
Souches E. coli disponibles: